資訊中心
作者:香雪生命科學(xué)研究中心--吳萬(wàn)里(翻譯轉載)
發(fā)布時(shí)間:2019-01-31
閱讀:11527
隨著(zhù)靶向腫瘤抗原TCR的鑒定及其對T細胞的轉導,有必要對其進(jìn)行功能驗證,以分析T細胞對同源肽或自體腫瘤細胞應答的靈敏性。靶向共有的組織分化抗原,如MART-1、gp- 100和CEA,可能對關(guān)鍵器官的正常細胞伴隨地產(chǎn)生毒性,因此,驗證TCR-T細胞對腫瘤的脫靶毒性也是必要的。盡管某些抗原不是廣泛表達的,如癌睪抗原NY-ESO-1和MAGE家族,它們表達在腫瘤組織,胎兒組織以及成人睪丸中,而在其他正常成人組織中不表達,但這些TCR-T細胞的安全性和親和力仍然需要被驗證。Parkhurst等人通過(guò)建立小鼠模型從脾細胞中分離出對CEA有反應的TCR并對其功能進(jìn)行驗證。在本研究中,他們證明了改良的CEA TCR是未來(lái)基因治療很好的候選基因,同時(shí)也展示了在TCR抗原結合區中選擇性的氨基酸替換可以提高TCR的反應親和力。Kunert等人從黑色素瘤患者中分離出針對4種MAGE-C2表位的10個(gè)TCR,并設計了一組驗證TCR-T細胞功能的實(shí)驗。Yao等人從MAGE-A3免疫后的兩名黑色素瘤患者PBMC中分離到的兩個(gè)MAGE-A3特異性的TCR,這些TCR識別由HLA-DPB1*04:01所遞呈的MAGE-A3抗原肽。通過(guò)比較這兩種TCR的特異性和親和性,發(fā)現6F9 TCR特異性地識別MAGE-A3,而不識別由HLA-DPB1*04:01所遞呈的MAGE-A家族的其它成員的抗原肽,因此,6F9 TCR被選做用于靶向MAGE-A3的MHC二類(lèi)限制性抗原肽的潛在的TCR基因治療。另一個(gè)問(wèn)題是,Kohn 等人揭示,許多在患者體內循環(huán)的改良T細胞沒(méi)有任何治療效果,是因為這些T細胞的逆轉錄表達活性是被降低了的。一些研究已經(jīng)報道了可能的方法來(lái)改善TCR的轉基因效果并提供一個(gè)穩定的免疫治療系統。Fujio等人使用兩個(gè)獨立的單順?lè )醋幽孓D錄病毒載體,最終得到卵清蛋白(OVA)特異性的TCR-T細胞,這些細胞顯示出了對抗原顯著(zhù)的應答反應。此外,攜帶雙向啟動(dòng)子的慢病毒載體在Bobisse等人的研究中使用,這個(gè)基因轉移系統顯示出更高的轉基因效率,表明慢病毒載體可能是免疫治療中TCR表達的有效工具。這些臨床前實(shí)驗有助于指導TCR-T細胞在臨床試驗中的應用,但是,對于新的靶向腫瘤抗原的TCR進(jìn)行親和性、毒性和安全性測試是必需的。
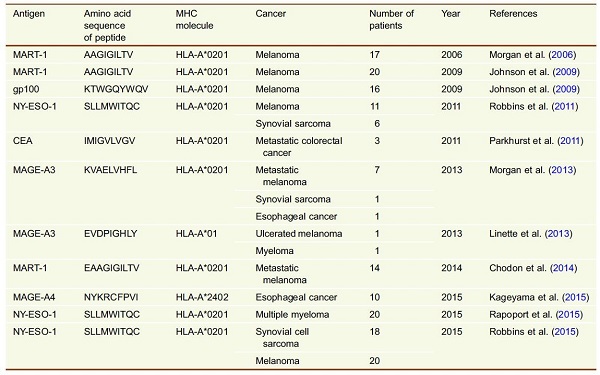
采用TCR-T的過(guò)繼免疫治療已成為癌癥治療的重要策略,最近的臨床試驗顯示出了令人鼓舞的結果(表1)。首次報道的是在2006年,MART-1 的TCR-T可以介導人類(lèi)腫瘤的消退,隨后,2009年和2014年MART-1 TCR-T的臨床試驗也證明了這一現象。Johnson等人指出,在使用gp100 TCR-T細胞治療的患者中,有19%的患者出現過(guò)抗腫瘤反應。除了分化抗原外,進(jìn)入臨床試驗的還有癌-睪抗原,如MAGE-A3和NY-ESO-1。在使用針對HLA-A*0201限制性NY-ESO-1抗原的TCR的臨床試驗中,有超過(guò)50%的滑膜肉瘤、黑色素瘤和骨髓瘤等患者被檢測到有應答反應。Kageyama等人進(jìn)行了一項臨床試驗,用針對HLA-A*2402限制性的、MAGE-A4的TCR-T檢測對食管癌的治療效果。通過(guò)檢測發(fā)現,這些TCR-T細胞可以在體內維持很長(cháng)一段時(shí)間,有3名患者維持最小腫瘤狀態(tài)超過(guò)27個(gè)月。這些臨床試驗表明,TCR-T細胞治療可使腫瘤發(fā)生明顯的消退。這引起了人們巨大的熱情,然而必須指出的是,大部分的臨床試驗只是在少數的癌癥患者中進(jìn)行。此外,盡管TCR-T在過(guò)繼細胞治療中取得了很大進(jìn)展,但也出現了一些意想不到的毒性。在一項靶向轉移性結直腸癌的TCR-T細胞臨床試驗中,所用的TCR對CEA有很高的親和力,結果三名患者均因TCR對表達CEA的正常結腸上皮細胞的反應而出現嚴重的暫時(shí)性結腸炎(盡管有1例患者在肺和肝臟的轉移癌出現了消退)。在另一項研究中,兩名患者在回輸TCR-T后死于心源性休克,該TCR靶向的是HLA-A*01限制性的MAGE-A3抗原。Linette等人通過(guò)在MAGE-A3 TCR的α鏈CDR-2區引入4個(gè)突變,β鏈保留用野生型序列,可以提高TCR的親和力,這種親和力增強的TCR可能會(huì )識別來(lái)自正常心臟組織表達的無(wú)關(guān)蛋白的表位,其野生型MAGE-A3特異性的TCR因為通過(guò)胸腺的自然選擇過(guò)程,也可能在患者體內擴增而沒(méi)有心臟毒性,在MAGE-A3的TCR-T治療后,兩名患者陷入昏迷,隨后死亡。在該研究中,經(jīng)基因改造的T細胞還識別了在人腦中被檢測到的MAGE-A12的衍生表位。由于潛在的交叉反應,TCR親和力的評估和合適抗原的選擇就需要非常的謹慎,這對TCR-T的安全臨床應用是非常必要的。
注:本文已獲得原文[1]作者(Ping Y)就原文翻譯以及網(wǎng)絡(luò )刊登的授權。 [1] Ping Y, Liu C, Zhang Y. T-cell receptor-engineered T cells for cancer treatment: current status and future directions [J]. Protein Cell, 2018,