資訊中心
作者:香雪生命科學(xué)-盧思遠
發(fā)布時(shí)間:2021-12-21
閱讀:11207
2019年年末,新型冠狀病毒肺炎((Corona Virus Disease 2019,COVID-19),簡(jiǎn)稱(chēng)“新冠肺炎”)疫情爆發(fā)開(kāi)始,目前已近兩年時(shí)間。近兩年來(lái),我們見(jiàn)證了成千上萬(wàn)醫務(wù)工作者逆行疫區的義無(wú)反顧,也見(jiàn)識了寒冬深夜里挑燈搭帳的核酸檢測。在疫情逐漸常態(tài)化的今日,我國不少居民都做過(guò)新冠核酸檢測,新冠疫苗接種覆蓋率已達70%以上,這有賴(lài)于我國藥品監督管理局對于疫情時(shí)期疫苗緊急使用的審批,使我國成為最早的疫苗接種國之一,為人民群眾的健康建立了牢固的屏障。

疫情爆發(fā)以來(lái),“臨床試驗”這以往相對陌生的名詞也越來(lái)越多地出現在人們的視野中。我國目前已有21個(gè)新冠疫苗進(jìn)入臨床試驗階段。有4個(gè)疫苗在國內獲批附條件上市,3個(gè)疫苗在國內獲批緊急使用,8個(gè)疫苗在國外獲批開(kāi)展Ⅲ期臨床試驗,1個(gè)mRNA疫苗在國外獲倫理批準。今天我們就來(lái)聊聊什么是“臨床試驗”?
一、臨床試驗概述
臨床試驗是指以人體(患者或健康受試者)為對象的試驗,旨在發(fā)現或驗證某種試驗用藥品的臨床醫學(xué)、藥理學(xué)以及其他藥效學(xué)作用、不良反應,或者試驗用藥品的吸收、分布代謝和排泄,以確定藥物的療效與安全性的系統性試驗。是新藥研發(fā)過(guò)程當中非常重要的組成部分。
新藥研發(fā),是一個(gè)投入高、周期長(cháng)的過(guò)程。據統計,一個(gè)新藥從化合物發(fā)現到獲批上市,往往需要持續數年甚至數十年,研發(fā)成本約為26億美元。新藥研發(fā)的過(guò)程主要分4個(gè)部分:(1)藥物發(fā)現:藥物基礎研究和應用篩選,以確定目標臨床試驗藥物;(2)臨床前研究:為確定藥物的藥理、藥代動(dòng)力學(xué)、有效性和安全性所進(jìn)行的動(dòng)物實(shí)驗;(3)臨床研究(臨床試驗):藥物人體藥代動(dòng)力學(xué)、安全性及有效性試驗;(4)新藥申請的申報與審批。
綜上所見(jiàn),臨床試驗是在新藥獲批前的重要階段。
二、藥物臨床試驗的目的與意義
1.評價(jià)新藥的臨床應用價(jià)值;
2.確定藥物在人體的安全性和有效性;
3.確定藥物在人體的藥代動(dòng)力學(xué)特征;
4.為新藥注冊和技術(shù)審評提供臨床依據。
三、臨床試驗的分類(lèi)
按照臨床試驗的一般規律,《藥物臨床試驗的一般考慮指導原則的通告》(2017年第11號)指出,按研究目的分類(lèi),將臨床試驗分為臨床藥理學(xué)研究、探索性臨床試驗、確證性臨床試驗、上市后研究。
1) 臨床藥理學(xué) 研究的目的是評價(jià)耐受性,明確并描述藥代動(dòng)力學(xué)及藥效學(xué)特征,探索藥物代謝和藥物相互作用,以及評估藥物活性。
2) 探索性臨床試驗 研究目的是探索目標適應癥后續研究的給藥方案,為有效性和安全性確證的研究設計、研究終點(diǎn)、方法學(xué)等提供基礎。
3) 確證性臨床試驗 研究目的是確證有效性和安全性,為支持注冊提供獲益/風(fēng)險關(guān)系評價(jià)基礎,同時(shí)確定劑量與效應的關(guān)系。
4) 上市后研究 目的是改進(jìn)對藥物在普通人群、特殊人群和/或環(huán)境中的獲益/風(fēng)險關(guān)系的認識,發(fā)現少見(jiàn)不良反應,并為完善給藥方案提供臨床依據。
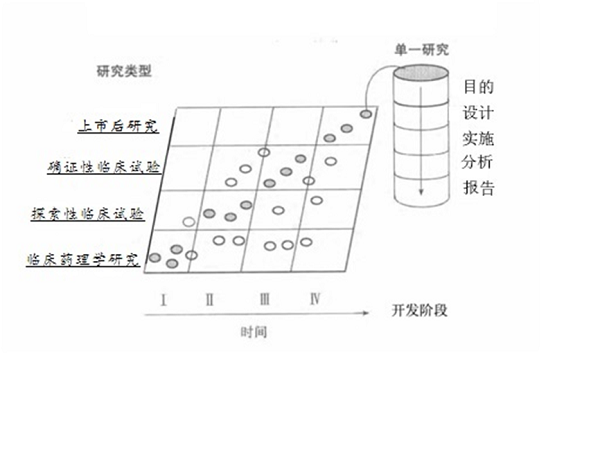
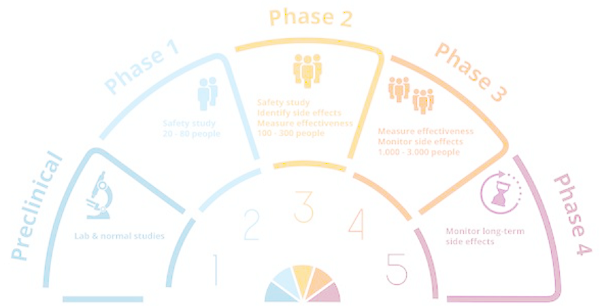
按研發(fā)階段分類(lèi),將臨床試驗分為Ⅰ期臨床試驗、Ⅱ期臨床試驗、Ⅲ期臨床試驗和Ⅳ期臨床試驗。
1) Ⅰ期臨床試驗 是新藥進(jìn)入人體試驗的起始期,其目的主要有兩個(gè):一是確定藥物在人體內的代謝和藥理學(xué)活性,觀(guān)察隨劑量增加出現的毒性,以及收集一些有效性的早期證據;二是獲取充分的藥代動(dòng)力學(xué)和藥理學(xué)作用的信息,為設計Ⅱ期臨床試驗提供依據。
2) Ⅱ期臨床試驗 當Ⅰ期臨床試驗提供了新藥的基本安全性信息后,進(jìn)入到藥效的初步評價(jià)階段。其目的是:①為了確定新藥作用于目標適應癥患者的最大和最低有效劑量范圍,為Ⅲ期臨床試驗劑量提供參考;②確定新藥產(chǎn)生療效的劑量-血藥濃度-藥效學(xué)指標的關(guān)系;③以更大的樣本量進(jìn)一步評價(jià)藥物的安全性。
3) Ⅲ期臨床試驗 Ⅲ期臨床試驗是治療作用確證階段。目的是進(jìn)一步驗證藥物對目標適應癥患者的治療作用和安全性,總體評價(jià)獲益風(fēng)險特征,最終為藥物注冊申請提供充分的依據。
4) Ⅳ期臨床試驗 Ⅳ期臨床試驗為新藥上市后應用研究階段。其目的是考察在廣泛使用條件下的藥物的療效和不良反應,評價(jià)在普通或者特殊人群中使用的獲益與風(fēng)險關(guān)系以及改進(jìn)給藥劑量等。
四、香雪生命科學(xué)技術(shù)(廣東)有限公司的臨床試驗
目前香雪生命科學(xué)技術(shù)(廣東)有限公司的一項治療腫瘤抗原NY-ESO-1表達陽(yáng)性(基因型為HLA-A*02:01)的以軟組織肉瘤為主的晚期惡性實(shí)體瘤患者的開(kāi)放、單臂、早期臨床研究正在開(kāi)展當中。該臨床試驗基于香雪生命科學(xué)技術(shù)(廣東)有限公司研發(fā)的具有完全自主知識產(chǎn)權的高親和力TCR技術(shù)平臺。同時(shí),更是我國首個(gè)獲批的治療軟組織肉瘤為主的實(shí)體瘤的TCR-T注冊臨床試驗。目前,公司也致力于更多新靶點(diǎn)、適應癥的研發(fā),相信在不久的將來(lái),將為廣大腫瘤患者帶來(lái)新的國際前沿治療技術(shù)。
全文參考:《藥物臨床試驗的一般考慮指導原則的通告(2017年第11號)》、《藥物臨床試驗管理學(xué)》等。