資訊中心
作者:香雪生命科學(xué)-郭珊珊
發(fā)布時(shí)間:2022-10-14
閱讀:10997
KRAS是一個(gè)近些年備受關(guān)注的人類(lèi)腫瘤相關(guān)基因家族,一系列高致死性癌癥都與其相關(guān),超過(guò)80%的胰腺癌、超過(guò)30%的結腸直腸癌膽管癌以及20%的肺腺癌都存在 KRAS 基因的激活突變,這是基因組中最重要的致癌突變之一。KRAS編碼一個(gè)小的 GTPase,作為精細調節的分子開(kāi)關(guān)發(fā)揮作用,通過(guò)在激活(GTP 結合)和失活(GDP 結合)構象之間循環(huán)來(lái)控制多個(gè)信號級聯(lián)通路,當細胞接受相關(guān)刺激時(shí),KRAS與 GTP 結合,它會(huì )“打開(kāi)”并激活細胞內信號通路,從而參與調控細胞增殖、分化、遷移、凋亡等生命活動(dòng),突變的KRAS 被組成型激活并持續“開(kāi)啟”,引起下游信號傳導失調并導致腫瘤發(fā)生。
KRAS 突變以單堿基錯義突變?yōu)橹鳎渲?/span> 98% 位于密碼子12(G12)、密碼子13(G13)或密碼子61(Q61),突變亞型主要分為KRAS(G12D)、KRAS(G12V)、KRAS(G12C)、KRAS(G13D)、KRAS(G12R)、KRAS(G12A)突變,研究表明,G12D 和G12V 突變是最常見(jiàn)的腫瘤突變類(lèi)型,G12D突變發(fā)生率在胰腺癌中最高,G12V 多發(fā)于卵巢癌,G12C是肺腺癌中最常見(jiàn)的,其他突變形式不太普遍。
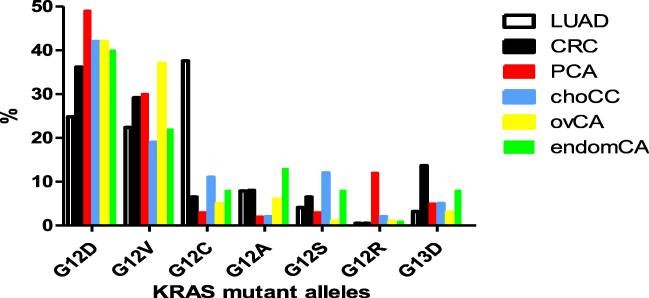
KRAS外顯子2突變等位基因在各種癌癥中的發(fā)生率(Timar J and Kashofer K,2020)數據以% 表示,LUAD肺腺癌,n = 579;CRC結直腸癌,n = 560;PCA胰腺癌,n = 2661;choCA膽管癌,n = 255;ovVA卵巢癌,n = 410;endomCA 子宮內膜癌,n = 306。
多年來(lái),KRAS 突變一直被認為是“不可治愈的”,一方面,KRAS 和 GTP 的親和力在 pM 水平,而 GTP 在細胞中的濃度高達 0.5 μM,很難像蛋白激酶抑制劑一樣實(shí)現有效競爭 ;另一方面,KRAS 蛋白沒(méi)有特征,它們具有近乎球形的結構,缺乏深疏水袋,并且沒(méi)有明顯的結合位點(diǎn)。
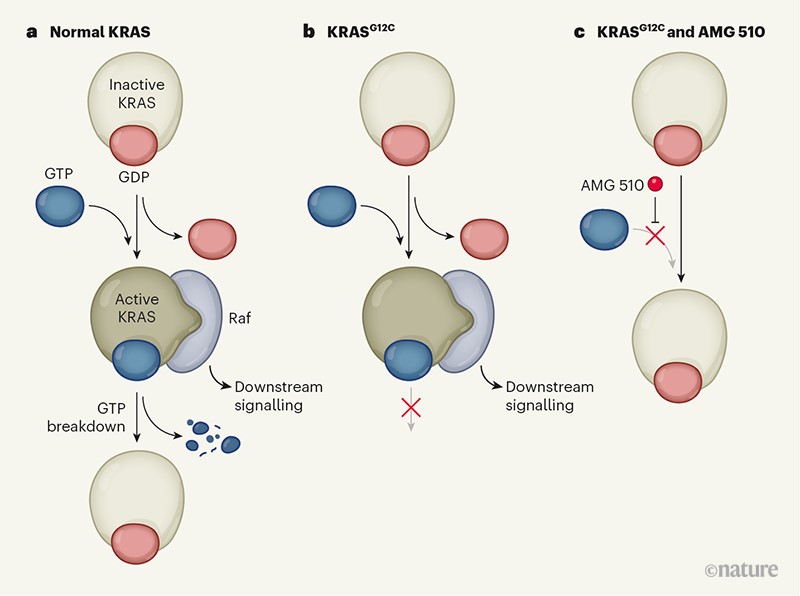
KRAS G12C突變體有一個(gè)從正常的甘氨酸(G)突變成半胱氨酸(C)的改變,該殘基已被用于設計有希望的共價(jià)抑制劑。2021年5月,美國FDA批準新型抗癌藥Sotorasib(AMG510)上市,這是全球首個(gè)上市的KRAS靶向藥,用于治療既往至少接受過(guò)一次系統治療的攜帶KRAS G12C突變的晚期或轉移性非小細胞肺癌患者,Sotorasib(AMG510)作為KRAS G12C的共價(jià)抑制劑,具有高選擇性和不可逆的特點(diǎn),可以將KRAS G12C 捕獲在非活性 GDP 結合狀態(tài)(下圖),臨床數據表明,Sotorasib治療對具有 KRAS G12C 突變且毒性可耐受的非小細胞肺癌患者具有顯著(zhù)療效,可代表一種新型靶向治療,但還需要進(jìn)一步的研究來(lái)確定Sotorasib 的耐藥機制、療效和安全性。此外,KRAS信號傳導的上游信號節點(diǎn)或下游傳導途徑的共抑制,或者聯(lián)合細胞周期檢查點(diǎn)共抑制,這些協(xié)同作用也在臨床試驗中進(jìn)行測試。
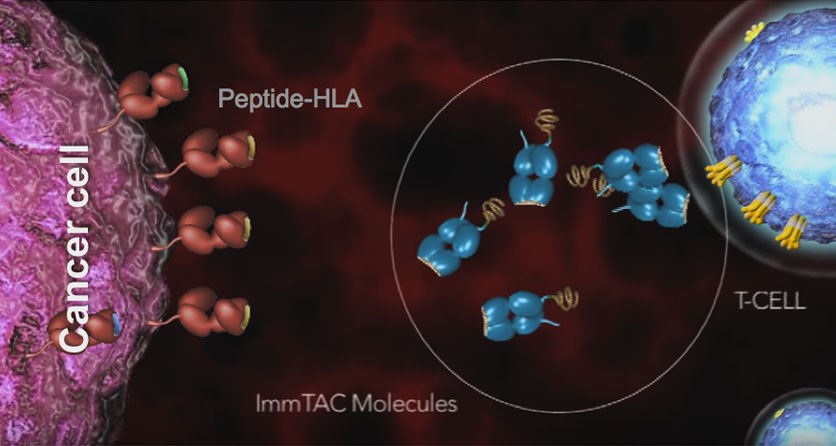
體細胞突變可以產(chǎn)生癌細胞特有的、正常組織中不存在的新抗原,使其成為免疫治療的有吸引力的靶標,宿主免疫靶向新抗原以引發(fā)內源性 T 細胞介導的抗腫瘤反應,盡管絕大多數體細胞突變是個(gè)體患者獨有的隨機突變,但致癌驅動(dòng)基因KRAS的部分突變形成了患者中常見(jiàn)的一類(lèi)共享新抗原。源自體細胞突變的新抗原對癌細胞具有特異性,是癌癥免疫治療的理想靶點(diǎn),目前,除了開(kāi)發(fā)針對KRAS G12C的靶向抑制劑,需要新的方法來(lái)治療由更頻繁的突變驅動(dòng)的癌癥,例如 KRAS G12D、KRAS G12V等。利用 T 細胞介導的腫瘤免疫提供了一種靶向癌癥特異性新抗原的治療方法,T 細胞可以通過(guò) T 細胞受體 (TCR)識別癌細胞表面人類(lèi)白細胞抗原(HLA)呈遞的新抗原衍生肽,具有KRAS G12D或KRAS G12V特異性的T 細胞克隆就可以用于免疫療法以抑制患者的腫瘤。
Andrew Poole(Andrew et al,2022)等人展示了一種親和力增強的 T 細胞受體(TCR)的識別和開(kāi)發(fā),他們分離得到HLA-A*11 (HLA-A*11-KRAS G12D)環(huán)境中針對 KRAS G12D十聚體肽(VVVGADGVGK)的特異人類(lèi)TCR ,通過(guò)對突變的TCR噬菌體文庫進(jìn)行親和力優(yōu)化獲得高親和力克隆,雖然晶體結構顯示 TCR 在KRAS WT與 KRAS G12D之間的相互作用幾乎沒(méi)有明顯差異,但是熱力學(xué)分析和分子動(dòng)力學(xué)模擬表明,TCR 特異性是由間接靜電相互作用的差異驅動(dòng)的,所以工程化 TCR 的親和力較野生型增加了4000倍,但完全能夠區分 KRAS G12D和 KRAS WT,制備與人源化抗 CD3 scFv 融合的親和力增強的可溶性雙特異性 ImmTAC 分子IMC-KRAS G12D,這是一種有效且特異性的 T 細胞接合劑,能夠介導 T 細胞活化并重定向 T 細胞靶向僅含有 KRAS G12D的癌細胞。
最近的證據表明,通過(guò) pHLA 通路直接靶向癌癥新抗原是可能的,新抗原代表了用 pHLA 特異性療法靶向癌細胞的機會(huì ),具有低腫瘤毒性風(fēng)險,提供對突變表位的選擇性保留。相關(guān)研究表明TCR可以檢測源自致癌突變的常見(jiàn)新抗原中的單個(gè)氨基酸突變, TCR 特異性的分子機制證明間接的能量驅動(dòng)因素可能導致野生型和突變的 KRAS G12D之間的親和力窗口增加 > 4000 倍,該窗口轉化為一種機制,通過(guò)該機制,具有親和力增強的 TCR 的 T 細胞結合 ImmTAC 分子可以實(shí)現對抗原陽(yáng)性癌細胞的良好特異性,同時(shí)保持對抗原陰性細胞的耐受性。這些發(fā)現證明了 TCR 療法對靶向新抗原的強大效用,并對理解新抗原治療性 TCR 選擇性的分子決定因素具有重要意義。
參考文獻:
Timar J and Kashofer K . Molecular epidemiology and diagnostics of KRAS mutations in human cancer .Cancer Metastasis Reviews,2020,39(4):1029-1038.
Poole A, Karuppiah V, Hartt A, et al; Therapeutic high affinity T cell receptor targeting a KRAS G12D cancer neoantigen. Nat Commun. 2022,13(1):5333.
Zhu C, Guan X, Zhang X, Luan X, et al; Targeting KRAS mutant cancers: from druggable therapy to drug resistance. Mol Cancer. 2022,21(1):159.
Canon J, Rex K, Saiki AY,et al. The clinical KRAS(G12C) inhibitor AMG 510 drives anti-tumour immunity.Nature. 2019 ,575(7781):217-223.